Dossier: Innovative tierversuchsfreie Forschung in Baden-Württemberg
Mini-Organe und Multi-Organ-Chips - wo Labormäuse vielleicht bald in Rente gehen
Tierversuche ade? Ein Blick auf die baden-württembergische Forschungslandschaft zeigt, wie Forschende in den Lebenswissenschaften neue Wege beschreiten, um im Sinne des 3R-Prinzips auf Tierversuche zu verzichten, sie zu reduzieren oder die Haltungsbedingungen für Tiere zu verbessern. Indem sie neue Modelle entwickeln und ein dichtes 3R-Netzwerk etablieren, investieren sie in die Zukunft und steigern gleichzeitig die Qualität der Ergebnisse. Das Ministerium für Wissenschaft, Forschung und Kunst (MWK) Baden-Württemberg unterstützt sie dabei mit insgesamt 6,9 Mio. Euro.
Experimente mit Tieren sind umstritten und wurden in den letzten Jahren zunehmend durch alternative Methoden wie In-vitro- und In-silico-Verfahren ersetzt. In Europa werden jedes Jahr schätzungsweise zwölf Mio. Tierversuche durchgeführt; viele aus traditionellen Gründen, da sie bei der Zulassung von neuen Medikamenten gesetzlich vorgeschrieben sind.
 In vielen Laboren in Baden-Württemberg bemühen
In vielen Laboren in Baden-Württemberg bemühen
sich Forschende in Baden-Württemberg bereits darum, das Tierwohl zu verbessern, indem sie neue Technologien entwickeln, die Tierversuche ergänzen oder überflüssig machen. Der Kaninchentest zur Testung fieberauslösender Substanzen wird im Jahr 2025 endgültig abgeschafft und durch neue Modelle ersetzt. © Fiona Heyl, FreiburgDie Anzahl der in Baden-Württemberg zu wissenschaftlichen Zwecken verwendeten oder getöteten Tiere war im Jahr 2022 mit 361.043 geringer als 2021 (393.760) und deutlich unter der von 2018 (533.685).
Tierversuche waren lange Zeit ein Eckpfeiler der medizinischen Forschung und haben zur Entwicklung zahlreicher lebensrettender Medikamente wie etwa Impfstoffen, Insulin oder Antibiotika beigetragen.
Bis ein Medikament marktreif ist, sind umfangreiche Präklinische Tests, oft an Tieren, zur Sicherheit und Wirksamkeit, vorgeschrieben. Das Genehmigungsverfahren für Tierexperimente ist streng reglementiert und soll sicherstellen, dass Tierversuche nur dann durchgeführt werden, wenn sie unbedingt notwendig sind. Oft ergibt sich daraus beim Versuch ein Methodenmix, in dem Tierversuche noch enthalten sind. Immer häufiger kommt es bei speziellen Fragestellungen jedoch schon zum vollständigen Ersatz durch alternative Methoden wie künstlich Organoide oder Organ-on-Chip-Modelle (OoC). Diese neuen Technologien ermöglichen es, die Sicherheit und Wirksamkeit von Medikamenten genauer und ethischer zu bewerten.
Der Mensch ist keine nackte 70 kg-Maus
Die Einschätzung über die generelle Eignung bestimmter Therapien stützt sich in der Präklinischen Phase hauptsächlich auf Tier- und 2D-Modelle. Schon oft scheiterten Tiermodelle jedoch bezüglich ihrer Übertragbarkeit auf den Menschen, denn Tier und Mensch unterscheiden sich in wesentlichen Merkmalen. Der Puls einer Maus liegt beispielsweise bei 600, der eines Menschen bei 70 bpm (beats per minute). Sie unterscheiden sich im Metabolismus und der Verträglichkeit von Substanzen, was zu gegensätzlichen Ergebnissen in Experimenten führen kann. Zudem leiden Tiere nicht an Zivilisationskrankheiten, die durch ungesunden Lebensstil verursacht werden. Für Tierversuche müssen Tiere erst krank gemacht werden. Um bei Ratten Depressionen hervorzurufen, versetzt man ihnen Elektroschocks, und Mäusen verschließt man Hirnarterien, um einen Schlaganfall zu simulieren. Dennoch werden damit die komplexen menschlichen Erkrankungen nicht adäquat wiedergegeben. Fatal ist, dass, wenn Prüfsubstanzen erst in späteren Studienphasen scheitern, sie Kosten in Millionenhöhe vergeuden. Wertvolle Wirkstoffkandidaten können gleichzeitig im Präklinischen Entwicklungsprozess verloren gehen, da sie am falschen Modell getestet wurden.
Erforschung humaner Krankheiten bedarf humanbasierter Modelle
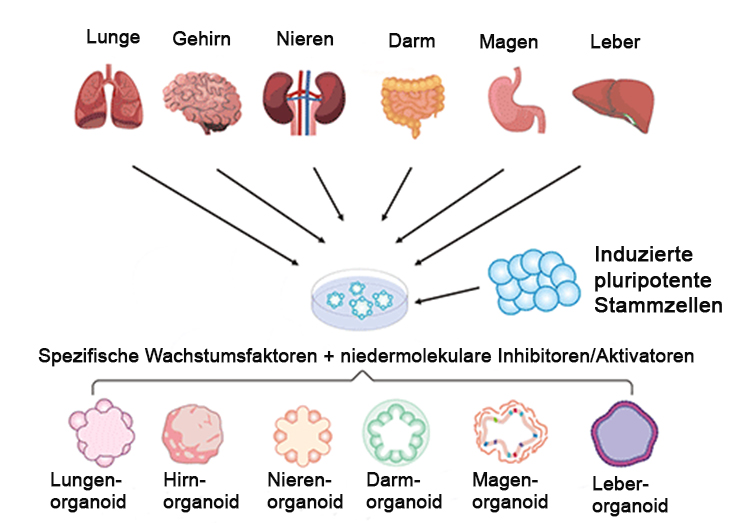 Aus Gewebeproben werden Zellen gewonnen, aus denen pluripotente Stammzellen generiert werden können. Mit ihnen und spezifischen Wachstumsfaktoren lassen sich nahezu sämtliche Organoide realisieren. © Stephanie Heyl, verändert nach https://www.cusabio.com/Organoids.html
Aus Gewebeproben werden Zellen gewonnen, aus denen pluripotente Stammzellen generiert werden können. Mit ihnen und spezifischen Wachstumsfaktoren lassen sich nahezu sämtliche Organoide realisieren. © Stephanie Heyl, verändert nach https://www.cusabio.com/Organoids.htmlOrganoide und Organ-on-Chips sind winzige dreidimensionale mikrophysiologische Systeme, die die Struktur und Funktion menschlicher Organe imitieren. Organoide bestehen aus verschiedenen sich selbst organisierenden Zelltypen, die unterschiedliche Funktionen übernehmen und miteinander wechselwirken. Ein Organoid besitzt die physiologische Architektur sowie die genetischen Eigenschaften des Spenderorgans. Es ähnelt gesundem oder spezifisch erkranktem Gewebe und ist damit für die Wirkstoffforschung in der Personalisierten Medizin sehr interessant. Organ-on-Chips sind mikrofluidische Systeme mit Nachbildungen funktioneller Einheiten eines Organs, wobei die Zellen in einer möglichst natürlichen Mikroumgebung miteinander interagieren. Das Nährmedium wirkt als Blutersatz und sorgt für Sauerstoff- und Nährstofftransport. Diese Methoden bieten eine höhere Humanrelevanz, sind meist deutlich kostengünstiger und liefern durch ihre Möglichkeit zum Hochdurchsatzscreening schnellere Ergebnisse für die wirksamste Therapie. Solche Methoden sind von Pharmafirmen geschätzt, da für sie weniger Prüfsubstanz benötigt wird.
Baden-Württemberg etabliert 3R-Netzwerk als erstes Bundesland
Das 3R-Prinzip (Replace, Reduce, Refine) ist in der EU zum besseren Schutz rechtlich verankert. Das Ziel: Tierversuche entweder vollständig ersetzen (Replace), die Zahl der Tiere auf ein Minimum reduzieren (Reduce) und ihr Leiden auf ein unerlässliches Maß beschränken (Refine). Gemeinsam mit den Hochschulen unterstützt das Ministerium für Wissenschaft, Forschung und Kunst (MWK) den Aufbau eines Netzwerks, das ganz Baden-Württemberg umspannt. Startschuss hierfür fiel 2020 mit der Einrichtung des 3R-Center für In-vitro-Modelle und Tierversuchsalternativen in Tübingen inklusive einer Brückenprofessur Organ-on-Chip der Uni Tübingen gemeinsam mit dem NMI Reutlingen. 2021 folgte per Ausschreibung die Einrichtung von vier weiteren Zentren am IZDG (Interdisziplinären Zentrum für Darmgesundheit) in Heidelberg, am CAAT-Europe (Center for Alternatives to Animal Testing) in Konstanz, ferner das 3R-Zentrum Rhein-Neckar in Heidelberg und Mannheim sowie das 3R-BioMedicUS in Stuttgart.
Außerdem wurden drei Forschungs- und zwei Lehrprojekte in Freiburg, Heidelberg, Reutlingen und Ulm gefördert. Seit August 2024 leitet Dr. Silke Riegger die Geschäftsstelle des Netzwerks und treibt dessen Vernetzung und Weiterentwicklung voran. Die Regionen Karlsruhe, Furtwangen und Ulm werden ab Januar 2025 durch die Förderung neuer Zentren zur Stärkung der 3R-Kompetenzen im wissenschaftlichen Nachwuchs beitragen.
Tierfreundliche Forschung im Ländle
 Leitet seit August 2024 die Geschäftsstelle des 3R-Netzwerkes in Baden-Württemberg und ist verantwortlich für weitere Vernetzung und Öffentlichkeitsarbeit: Dr. Silke Riegger. © Dr. Silke Riegger, Werbefotografie Patrick Hipp.
Leitet seit August 2024 die Geschäftsstelle des 3R-Netzwerkes in Baden-Württemberg und ist verantwortlich für weitere Vernetzung und Öffentlichkeitsarbeit: Dr. Silke Riegger. © Dr. Silke Riegger, Werbefotografie Patrick Hipp.Mit Einrichtung des ersten 3R-Centers in Tübingen sowie der Brückenprofessur für Prof. Dr. Peter Loskill sind Entwicklung und Anwendung von Organ-on-Chip-Systemen gefördert worden. Für die Entwicklung dieser OoCs ist der Forscher gemeinsam mit Dr. Silke Riegger 2024 mit dem Ursula M. Händel-Tierschutzpreis ausgezeichnet worden, mit 80.000 Euro einer der höchstdotierten Forschungspreise dieser Art in Deutschland. Forschende um Loskill entwickelten ein Brustkrebs-on-Chip-Modell, mit dem sich die Interaktion des Tumors mit Immunzellen, die Zytokinfreisetzung sowie die Wirksamkeit von CAR-T-Zellen untersuchen lassen. Auch werden an einem Retina-on-Chip verschiedene Medikamente auf Sekundärtoxizität getestet, um mögliche Nebenwirkungen zu finden. Eine Core Facility für mikrophysiologische System an der Uni Tübingen bietet außerdem einen niederschwelligen Zugang zur Technologie. Zur Verbreitung gibt es ein 3R-Modul für Studierende, alle zwei Jahre eine Konferenz (THE 3R-LÄND) und überregional die EUROoCS-Konferenz (European Organ-on-Chips Society).
Im 3R-Zentrum Rhein-Neckar an der Uni Heidelberg und dem Zentralinstitut für Seelische Gesundheit (ZI) Mannheim erweitert man das Prinzip auf 6R für noch mehr Tierwohl: hinzu kommen Registration (Registrierung schon vor Beginn der Studie), Reproducibility (Wiederholbarkeit der Ergebnisse) und Reporting (auch Veröffentlichung von Negativergebnissen). Hier kümmern sich Forschende um ein besseres Handling der Mäuse sowie eine Klassifizierung zur Belastung von Tierversuchen. In einem MRT-Scanner können Nagetiere schmerzfrei untersucht werden. Dr. Marcus Meinhardt, Leiter des Instituts Psychopharmakologie am ZI und Koordinator des 3R-Zentrums Rhein-Neckar, evaluiert neue Wirkstoffkandidaten bei Substanzstörungen und bietet das 3R-Zentrum als Anlaufstelle für das Design neuer Tierexperimente auch in silico an.
Prof. Dr. Monilola Olayioye, Sprecherin des 3R-BioMedicUS Stuttgart, entwickelt 3D-Tumormodelle, die die komplexe Heterogenität des humanen Tumors widerspiegeln. Im 3R-BioMedicUS kommen dabei auch hochpräzises Bioprinting (Tissue Engineering) aus Biomaterial und Zellen sowie Leitgefäße aus Pflanzen als Blutgefäßmodelle zum Einsatz. Ebenso in Stuttgart entwickelt Dr. Anke Burger-Kentischer am Fraunhofer IGB ein 3D-Hautmodell, mit dem sich durch ein in die Zellen eingebautes Reportergen die direkte Reaktion auf Substanzen ablesen lässt. Hierfür bekam sie gemeinsam mit Beiersdorf 2024 den Hamburger Forschungspreis für Alternativmethoden zum Tierversuch.
Das 3R-Center NAM-ACCEPT am CAAT-Europe in Konstanz hat als Kernbereich Prüfstrategien zur Erfassung von Entwicklungsneurotoxizität. Hierzu entwickelte Prof. Dr. Marcel Leist basierend auf menschlichen Zellen eine tierfreie Testbatterie, mit der im Hochdurchsatzverfahren bereits knapp 200 Substanzen getestet wurden. Außerdem sind In-vitro-Neuronenmodelle etabliert worden, die biokinetische Prozesse wie die Wirkstoffverteilung zeigen, und deren Ergebnisse in mathematischen Modellen analysiert werden. Mit dem hier etablierten humanbasierten Monozyten-Aktivierungstest (MAT) lässt sich seit Jahren zuverlässig feststellen, ob Arzneimittel fieberauslösende Substanzen enthalten. Ab Juli 2025 wird dieser Test den bisherigen Kaninchentest vollständig ablösen.
 Auf dem Cervix-on-Chip ist das Modell eines Gebärmutterhalses entwickelt worden. Die Versorgung sowie der Abtransport von Stoffen ist durch die kleinen Kanälchen gewährleistet. © 3R-Center Tübingen
Auf dem Cervix-on-Chip ist das Modell eines Gebärmutterhalses entwickelt worden. Die Versorgung sowie der Abtransport von Stoffen ist durch die kleinen Kanälchen gewährleistet. © 3R-Center TübingenDurch Bioprinting werden im Reutlinger 3R-BioMED-Lab Leberzellen in Chips integriert, um die hepatotoxische Wirkung von Medikamenten zu testen. Zahlreiche andere OoC-Systeme sind hier ebenfalls entwickelt worden. Ein wichtiger Kernbereich ist die Veröffentlichung von Projektergebnissen in Youtube-Videos von und für Studierende. Außerdem setzt man in Reutlingen auf die In-vitro-Erzeugung nachhaltiger Fischlebensmittel, die in Wertigkeit und Geschmack mit echten Fischprodukten mithalten und weder mit Giften noch Medikamenten belastet sind.
Am Uniklinikum Freiburg ist eine tierfreie Sicherheitsbeurteilung für zellbasierte Krebstherapien entwickelt worden. Damit lässt sich beobachten, wie CAR-T-Zellen das Zytokinfreisetzungssyndrom beeinflussen. Ein weiterer Schwerpunkt liegt auf der Entwicklung von Modellen zur Vorhersage von Rückenmarksverletzungen, bei denen wissenschaftliche Verzerrungen systematisch reduziert werden.
Acht baden-württembergische 3R-Zentren am Start
Am neu gegründeten iR-Centre (integrative und innovative Ersatzmethoden) in Ulm entsteht ein neues Refinement-Labor mit Fokus auf Tumor- und Traumaforschung, in dem kontinuierlich die Tierbelastung (z. B. am Cortisolwert) kontrolliert wird. Außerdem werden hier Organoidtechnologien weiterentwickelt sowie eine Biobank zum Austausch von tierischem Gewebe eingerichtet. Prof. Dr. Alexander Kleger, Spezialist für Bauchspeicheldrüsenkrebs, identifiziert mit Pankreasorganoiden Biomarker, die den Tumor frühstmöglich anzeigen. Auch hier gibt es eine Core Facility Organoide, in der Forschende Organoide etablieren, kultivieren sowie auf Stoffe testen können.
Ebenso eröffnet im Januar 2025 das 3ROCKIT in Karlsruhe, das den Fokus auf Computermodelle legt. Die Idee ist die Erstellung digitaler Zwillinge sowie autonome Labore zur Erforschung von In-vitro-Methoden.
Das Entwicklungs- und Transferzentrum für 3D-Gewebemodelle in Furtwangen wird Tests für Pharmazeutika an künstlich nachempfundener Knochensubstanz und Haut durchführen und besonders ein interdisziplinäres Lehr- und Beratungsangebot für Studierende anbieten. Prof. Dr. Margareta Müller, zukünftige Leiterin des neuen Zentrums, ist seit 30 Jahren auf In-vitro-Modelle als Tierersatz spezialisiert und sagt: „Es ist wichtig, dass der wissenschaftliche Nachwuchs von vornherein eine Expertise in 3R entwickelt.“
Die Kombination von Organoiden, OoC-Technologien, Computersimulationen und epidemiologischen Studien verspricht aussagekräftigere Ergebnisse als Tierversuche. Eine bessere Vernetzung und der Austausch von Expertise sind entscheidend für den Erfolg dieser neuen Methoden.
Welche Tiere kamen 2022 zu welchen Zwecken zum Einsatz?
Deutschlandweit wurden überwiegend Mäuse eingesetzt (72 %), der kleinere Anteil verteilte sich auf Fische, Ratten, Kaninchen und Vögel. Die absolute Zahl der genetisch veränderten Tiere ist gesunken, ihr Anteil an der Gesamtzahl der Tiere jedoch gestiegen. Über die Hälfte der Versuche dienten der Grundlagenforschung, ein kleinerer Teil der Erforschung von Krankheiten sowie der Qualitätskontrolle und Sicherheitsprüfung von medizinischen Produkten. In der angewandten Forschung bezog sich der Hauptteil der Tierversuche mit Abstand auf Krebserkrankungen (42 %), gefolgt von Nerven- und Geisteserkrankungen (12 %) und Infektionskrankheiten (10 %).